


Voici un bilan des 10 dernières années sur les avancées de la chimie. On se rend compte que le monde moléculaire devient de plus en plus précis et que nos connaissances des mécanismes de transformation de la matière commencent par être connus au plus profond de l’atome.
2016 :
Jean-Pierre Sauvage (France), J.Fraser Stoddart (Ecosse) et Bernard L.Feringa (Pays-Bas)
pour leurs travaux sur la conception et la synthèse de machines moléculaires.
2015:
Aziz Sancar (Turquie/Etats-Unis), Paul Modrich (Etats-Unis) et Tomas Lindahl (Suède)
pour leurs travaux sur la réparation de l’ADN.
2014:
Eric Betzig et William Moerner (Etats-Unis), et Stefan Hell (Allemagne),
qui ont amélioré le microscope, lui permettant de voir l’infiniment petit.
2013:
Martin Karplus (Etats-Unis/Autriche), Michael Levitt (Etats-Unis/Grande-Bretagne) et Arieh Warshel (Etats-Unis/Israël),
pour la mise au point de modèles pour les systèmes chimiques complexes permettant d’optimiser les catalyseurs, les médicaments et les cellules photovoltaïques.
2012:
Robert Lefkowitz et Brian Kobilka (Etats-Unis),
pour leurs travaux sur des récepteurs qui permettent aux cellules de comprendre leur environnement, une percée essentielle pour l’industrie pharmaceutique.
2011:
Daniel Shechtman (Israël),
pour avoir découvert l’existence d’un nouveau type de matériau, un “quasi-cristal”.
2010:
Richard Heck (Etats-Unis), Ei-ichi Negishi et Akira Suzuki (Japon),
pour avoir créé l’un des outils les plus sophistiqués de la chimie ouvrant la voie à des traitements du cancer et à des produits électroniques et plastiques révolutionnaires.
2009:
Venkatraman Ramakrishnan, Thomas Steitz (Etats-Unis) et Ada Yonath (Israël),
pour leurs travaux sur les ribosomes qui ouvrent la voie à de nouveaux antibiotiques
2008:
Roger Tsien, Martin Chalfie (Etats-Unis) et Osamu Shimomura (Japon)
pour leurs recherches sur les protéines fluorescentes dont les applications permettent de détecter des tumeurs cancéreuses
2007:
Gerhard Ertl (Allemagne)
pour ses travaux sur les catalyseurs qui ont connu des applications industrielles allant des fertilisants aux pots catalytiques
2006:
Roger Kornberg (Etats-Unis),
pour ses travaux fondamentaux sur la transcription des gènes

L’heure de l’apéro est LE rendez-vous quotidien qui agrémentent nos périodes de vacances estivales avec les beaux jours. Même si je ne suis pas un aficionados du Pastis, il est un phénomène étrange mais tout à fait explicable qui survient régulièrement autour des traditionnelles cacahuètes et autres amuse-gueules.
Pourquoi le Pastis, qui est d’ordinaire un liquide transparent jaunâtre devient-il opaque et laiteux lorsqu’on y ajoute de l’eau ?
Et bien figurez-vous qu’il s’agit là d’un phénomène chimique tout à fait intéressant.
De quoi le Pastis est-il fait ?
Dans un premier temps, il est impératif de comprendre la composition du Pastis.
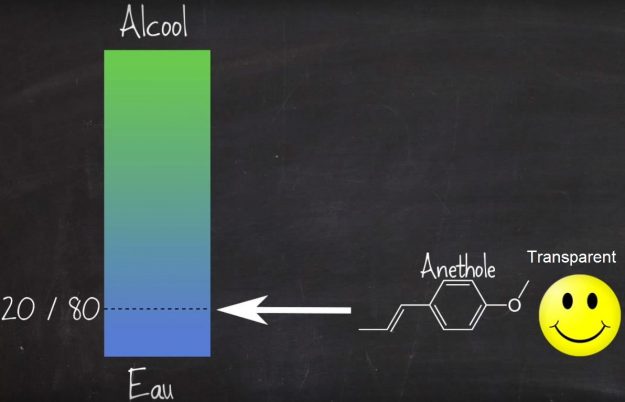
Sans vouloir rentrer dans des secrets de fabrication, on va admettre que ce soluté, lorsqu’il est pur, est composé de 50% d’alcool et de 50% d’eau (même si on se doute qu’il y a quelques petits produits ajoutés mais qui n’entrent pas dans le mécanisme physico-chimique de la transformation à l’inverse de la Vodka qui n’est composée que d’alcool et d’eau). Dans cet alcool, on trouve un composé particulier qui se nomme l’Anéthole (voir schéma ci-dessous), composé organique obtenu par extraction de l’anis.
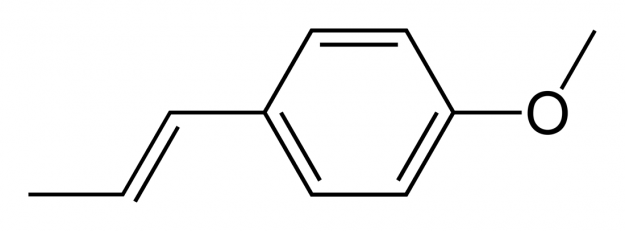
C’est se composé qui donne son goût à l’anis et au fenouil. C’est une substance qui est treize fois plus sucrée que le sucre et qui présente la particularité d’être transparente lorsqu’elle est placée dans un milieu équilibré en alcool et en eau ce qui est le cas dans une bouteille de Pastis (voir schéma ci-dessous).
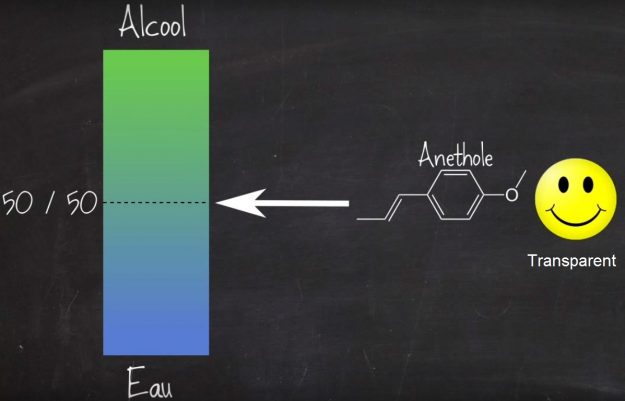
On trouve ce composé dans les alcools du bassin méditerranéen comme le Raki en Turquie, l’Ouzo en Grèce et le Sambuca en Italie.
C’est seulement lorsqu’on déséquilibre le rapport alcool/eau que la solution devient opaque (voir schéma ci-dessous).
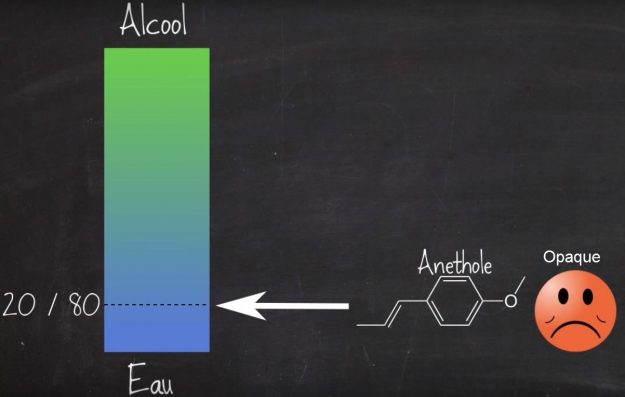
Que se passe-t-il ?
Le mystère est entier car on mélange deux liquides qui sont transparents et on obtient une solution qui est opaque !
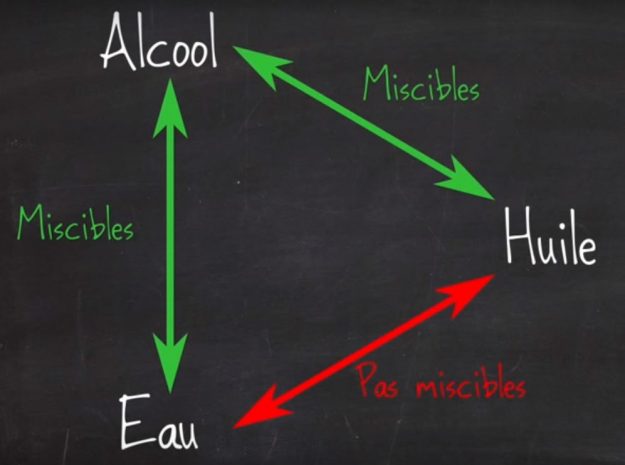
L’Anéthol est un composé hydrophobe, c’est à dire qu’il n’est pas miscible à l’eau (que l’on ne peut pas mélanger) il est même considéré comme étant une huile essentielle. L’Anéthole ne se mélange donc pas avec de l’eau néanmoins comme l’indique le schéma ci dessous, il accepte de se mélanger avec de l’alcool lorsque l’équilibre alcool/eau est atteint.
Lorsque l’on rajoute de l’eau à la solution, un déséquilibre se crée et l’Anéthole refuse de se mélanger. Les molécules d’Anéthole vont alors se regrouper entre elles et former des amas moléculaires d’Anéthole en suspension. On parle d’émulsion d’Anéthole, des gouttes d’huile se regroupent et donnent au pastis son aspect laiteux bien connu.
La diffusion de Mie
Voilà un phénomène physico-chimique bien particulier et qui apparaît lorsque des particules ont une taille dont l’ordre de grandeur est égale ou plus grande que la longueur d’onde du rayonnement qui les frappent.
Je m’explique.
La lumière est une onde. elle possède donc une longueur d’onde qui est comprise entre 400 nm (nanomètre) pour le bleu et 800 nm pour le rouge. Lorsque la lumière va heurter des particules dont le diamètre est compris entre 400 et 800 nm alors le phénomène de diffraction de Mie apparaît et de ce fait, le rayonnement est renvoyé dans toutes les directions. On dit qu’elle est diffusée.

Dans notre Pastis allongé, les gouttelettes d’Anéthole font quelques microns de diamètre. Lorsque la lumière visible rencontre ces gouttelettes, elle se trouve diffusée dans toutes les directions et c’est ce phénomène qui provoque l’aspect laiteux de la solution. On retrouve cet aspect avec le lait qui contient bon nombre de gouttelettes de graisse en suspension dans de l’eau et c’est à cause de la diffusion de Mie sur ces gouttelettes que le lait a cet aspect blanc et opaque. On retrouve ce phénomène avec les nuages dans lesquels se sont des gouttelettes d’eau qui sont dispersées dans de l’air. De même, les poussières et polluants dans l’atmosphère au-dessus des grandes villes diffusent le rayonnement solaire à toutes les longueurs d’onde. Sur la photo ci-dessous de la ville de Curitiba (Etat du Paraná au Brésil), on peut observer un nuage grisâtre du à la diffusion de Mie.

Voilà, vous savez désormais pourquoi lorsqu’on verse de l’eau dans votre Ricard, ce dernier devient opaque.
Contre expérience !
Prenez un verre de Pastis dans lequel vous avez versé de l’eau. Il devient donc opaque. Versez ensuite un peu de liquide vaisselle et mélangez vigoureusement. Que se passe-t-il ?
Le pastis redevient transparent !
Si l’on fait la même expérience avec de l’huile mélangée à de l’eau, on arrive a mélanger l’huile et l’eau. Le liquide vaisselle permet de réduite légèrement la tension qui existe entre les gouttelettes d’huile et les molécules d’eau.
Dans le cas du Pastis allongé, on améliore la compatibilité entre l’Anéthole et l’eau, les gouttelettes d’huile se cassent, la diffusion disparaît la lumière peut à nouveau traverser le mélange et la solution redevient claire…
Mais elle est imbuvable j’en conviens ! Raison de plus pour s’en servir un autre !

Un peu d’histoire…
La première guerre mondiale sonne le glas de l’ABSINTHE, boisson numéro un de la fin du XIXème siècle, anisé populaire, bouc émissaire de la lutte anti-alcoolique, cible numéro un du lobby viticole ressuscité du phylloxéra (parasite de la vigne). En 1914, tout alcool titrant plus de 16° est rigoureusement interdit. Il faudra attendre la fin de la guerre pour que ceux ci soient réautorisés, l’ABSINTHE exceptée, (interdite par décret en 1915). Mais l’habitude de l’anisé, frais, mélangé à l’eau va persister. En 1920, l’État français autorise les anisés, jusqu’à 30° d’alcool (de peur que l’ABSINTHE ne refasse surface).
Autour de MARSEILLE, la tradition de l’apéro est bien vivante : eau fraîche, anis et réglisse se marient et s’enrichissent d’autres macérations de plantes aromatiques. Il existait déjà des ABSINTHES marseillaises à base de badiane et de réglisse (anis étoilé plutôt qu’anis vert). Le rythme et la «bonne vie provençale» vont donc favoriser très naturellement une production de ces apéritifs anisés, sans cesse réinventés au gré des inspirations des patrons de bar et des marchands de vin, et ceci dans une totale illégalité.
A la fin des années 20, un jeune commercial de 23 ans, fils d’un négociant en vin, s’empare de l’idée et, coup de génie, commercialise un apéritif anisé à son nom. Bravant les autorités, Paul RICARD distribue largement cet alcool interdit. Il est constamment mis à l’amende par les autorités de police et de douane. Après un intense travail de lobbying, il obtient par décret en 1932 l’autorisation d’exploitation. Les amendes sont donc transformées en taxes. Paul RICARD devra trouver un nom à sa boisson et sera sommé de la définir. Sa recette est donc dans le domaine public et se nommera «PASTIS», du provençal «pastisson» et de l’italien «pasticchio», synonyme de mélange, d’amalgame. Le PASTIS est officiellement né. Paul RICARD aura commercialement trois ans d’avance sur la concurrence. Le succès est fulgurant.
PERNOD, l’initiateur de l’ABSINTHE en France profite de l’autorisation en sortant son «PERNOD» mais n’indiquera pas l’appellation PASTIS sur ses bouteilles.
Pourtant, il s’agit bien d’un anisé de la même famille.
En 1936, les premiers congés payés popularisent définitivement le PASTIS et l’instituent comme premier apéritif en France. Et enfin, en 1938, RICARD obtient pour tous les anisés l’autorisation de commercialiser à 45° au lieu de 40°.
Durant la seconde guerre mondiale, les alcools au-dessus de 16° sont à nouveau interdits. Il faudra attendre 1951 pour que soient réautorisés le PASTIS et tous les autres alcools forts. PERNOD engage enfin la riposte et sort son 51 avec l’appellation «PASTIS DE MARSEILLE». La guerre est engagée entre les deux producteurs jusqu’à ce qu’en 1974 un rapprochement et une fusion aient lieu sous l’impulsion des dirigeants des deux entreprises. Le groupe PERNOD RICARD aura le succès et l’extension qu’on lui connaît. Il verrouillera le marché en terme de volume de vente, même si une multitude de petits PASTIS voient le jour. Toutes les distilleries d’ABSINTHE survivantes sortiront leurs boissons anisées avec en tête le fameux «PONT» de PONTARLIER, distillation d’anis vert en tête.
A la fin des années 80 apparaissent des PASTIS différents, plus complexes, mélanges aromatiques élaborés par macération. HENRI BARDOIN en sera l’instigateur, suivi de près par JEAN BOYER, JANOT etc…
Le PASTIS nouveau est né. Inspiration, créativité et tradition, l’horizon s’ouvre sur une infinité de mélanges subtils, d’une richesse insoupçonnée. Ils rivalisent avec les vins. La palette est fabuleuse.
Mes remerciements à :
Marie-Claude Delahaye, Jacques Sallé, Martine Nouet

On me demandait dernièrement quels étaient les mécanismes entrant dans la fabrication de la mayonnaise. Ce à quoi je répondis comme si de rien n’était:”ben, c’est juste un problème d’émulsion nécessitant l’ajour de produits tensioactifs…” En examinant les yeux horrifiés de mon interlocutrice, je décidais de reprendre ma blouse d’enseignant et de lui expliquer le plus simplement possible.
L’émulsion est à la base un mélange fondamentalement hétérogène, mais pas nécessairement, de deux liquides non miscibles (que l’on ne peut pas mélanger), par exemple l’eau et l’huile, dont l’un forme des gouttelettes microscopiques en suspension dans l’autre grâce à l’action d’un “émulsifiant”.
L’émulsion est en fait une dispersion de gouttelettes d’huile (qu’on appelle aussi micelles) dans l’eau. Mais nous savons que lorsque l’on essaie de mélanger de l’huile et de l’eau, automatiquement les deux phases se séparent, l’eau étant plus dense en dessous, et l’huile, plus légère au dessus.
C’est la que l’émulsifiant encore appelé “tensioactif” entre en scène.
De quoi sont composées les molécules d’eau et d’huile?
Les molécules d’eau sont composées d’un atome d’oxygène relié à deux atomes d’hydrogène. Les molécules d’eau se relient entre elles grâce aux actions des liaisons hydrogènes, entre un atome d’oxygène d’une molécule d’eau et un atome d’hydrogène d’une molécule d’eau voisine. La molécule d’eau est qualifiée de polaire car elle possède un pôle chargé négativement et un autre positivement. En réalité, il suffit de se dire qu’il y a plus d’électrons dans l’atome d’oxygène que dans celui d’hydrogène et que, par conséquent, l’oxygène tend naturellement à être plus chargé négativement que l’Hydrogène. Et comme les charges négatives attirent les charges positives, il y a une grande affinité entre les atomes d’oxygène et ceux d’hydrogène (voir figure ci-dessous). L’affinité étant représentée par des traits en pointillés.
Les molécules d’huile, sont essentiellement formées d’atomes de carbone et d’hydrogène. Ce sont des molécules appelées triglycérides (les mêmes que celles qui circulent dans notre sang !), c’est à dire qu’elles forment un peigne à trois dents.
Mais alors pourquoi ces molécules ne peuvent pas ce mélanger ?
L’eau nous l’avons vu est une molécule polaire, c’est à dire qu’elle a un pôle possédant des charges positives (côté hydrogène) et un autre des charges négatives (côté oxygène). La molécule d’huile est quant à elle est dite apolaire. Elle ne présente pas de zones chargées positivement et négativement à sa surface. Il lui est donc impossible de se stabiliser avec les molécules d’eau car elle ne peut pas former de liaisons hydrogène avec celle-ci.
Que faire pour que les deux phases se mélangent ?
Il faut donc ajouter un « émulsifiant ». Il est composé de molécules tensio-actives. Ce sont des molécules qualifiées d’amphiphiles, c’est-à-dire qu’on retrouve deux parties de caractéristiques différentes, une partie est dite lipophile (c’est-à-dire qu’elle “aime” et retient les matières grasses) et est apolaire, l’autre est qualifiée d’hydrophile (c’est-à-dire miscible dans l’eau) et est polaire. Ces molécules vont englober des gouttelettes d’huile appelées micelles, en mettant à leur contact leur partie lipophile, et disperser ces gouttelettes enrobées dans l’eau, en se liant aux molécules d’eau grâce à leur partie hydrophile.
On peut représenter ce résultat avec le schéma suivant:
Un exemple en cuisine:
Nous pouvons observer l’exemple de la mayonnaise.
Pour réaliser une mayonnaise, On doit mélanger de l’huile, du jaune d’oeuf et de la moutarde. Les molécules tensioactives (ici la lécithine) sont données par le jaune d’œuf et par la moutarde. Il peut donc se produire une émulsion entre les molécules d’huile et d’eau. En plus de la présence de ces trois éléments la réussite de la mayonnaise dépend aussi de paramètres physico-chimiques: La température par exemple (les produits doivent être à température ambiante), le pH aussi (un pH un peu acide favorisera la réaction. On peut donc rajouter du jus de citron ou du vinaigre), la taille des micelles également (Si les micelles sont petites, la mayonnaise sera plus stable, une mayonnaise fortement et longuement battue sera plus stable qu’une mayonnaise légèrement battue).Ces paramètres physico-chimiques influencent ainsi le goût de la mayonnaise.
Où trouver des molécules tensioactives ?
On trouve aussi d’autres produits tensioactif : la phosphatidylcholine aussi connue sous le nom de lécithine, le sulfate laurique de sodium, ce sont des produits comestibles mais aussi les sulfonamides utiles dans le traitement de l’eau calcaire, les sels d’ammonium…
Une anecdote… Je n’ai jamais réussi à faire une mayonnaise correcte dans ma cuisine… heureusement, mon épouse s’en charge avec talent !
Et maintenant, A table !
La chimie, c’est la science des transformations. Elle a permis la synthèse de nombreux produits (en pas que la méthamphétamine !) qui ont profondément modifié notre vie quotidienne. Sans chimie, plus de matériaux, de céramiques (porcelaine, verre…), de ciment, de mortier… de maisons. Nous vivrions encore dans des cavernes, mangerions avec les doigts et boirions dans le creux de nos mains.
Sans chimie, plus de papier, d’encre… La transmission des connaissances se ferait uniquement par voie orale.
Ces synthèses bien sur nécessitent une compréhension fine de la réaction chimique, acquise au cours des deux derniers siècles.
Les chimistes du 19ème siècle, qui ne pouvaient “voir” les atomes, ont réussit cependant à déterminer les structures par analyse chimique.
Un grand thème du 20ème siècle a été la compréhension des mécanismes, qui précisent comment les structures se transforment au cours d’une réaction.
Comme les intermédiaires ne peuvent être isolés et étudiés, élucider un mécanisme revient à regarder les premières et dernières scènes d’une pièce de théâtre et à deviner ce qui se passe entre les deux.
Et on y arrive !
Le 21è siècle verra sans doute une chimie des systèmes complexes, ayant des caractéristiques proches du vivant.
La chimie est née à la fin du 18ème siècle quand l’homme ne s’est plus contenté de recettes empiriques, et qu’il a cherché à comprendre ce qu’il faisait, et ce qu’il voyait, ce qui nécessitait de répondre à plusieurs questions.
Imaginez Sherlock Holmes dans une situation embarrassante :

C’est incroyable et peu crédible non ? et pourtant c’est ce qu’on fait les chimistes du 19ème siècle.
Ce fut là le génie de ces hommes et femmes (plus tard) qui ont ouvert la porte d’une discipline scientifique encore aujourd’hui en pleine expansion.
Vous aimeriez vous lancer corps et âme dans la chimie ?
Vous pensez que demain, en ajoutant un liquide rouge et fumant à un autre liquide bleu plein de bulles vous créerez un truc vert qui explosera au contact de l’eau ? Eh bien non, désolé.
Je sais, je dis ça de façon un peu cruelle, mais comprendre la chimie, ça prend du temps. Bien que ça soit une matière très logique, il faut y aller doucement et beaucoup pratiquer, et vous n’êtes pas encore prêt de risquer de faire exploser votre garage lors d’une expérience.
Avant toute chose, il me semble important de vous expliquer ce qu’est exactement la chimie, à quoi ça sert, et pourquoi c’est une science à part entière. Vous verrez bientôt qu’elle est présente dans notre vie de tous les jours…
Citation : Le petit Larousse illustré, édition 2007 : “Science qui étudie la constitution atomique et moléculaire des corps, ainsi que leurs interactions.“
Mouais… C’est juste, mais un peu léger non ?
Personnellement, je vais tenter de vous expliquer ça à ma façon. La chimie est donc tout d’abord une science, tout comme les mathématiques, la physique ou la biologie. Cette science s’intéresse à la nature de la matière : la façon dont elle est constituée, comment elle réagit dans un milieu donné, etc. Elle s’intéresse donc aussi à l’évolution de cette matière si on la met en contact avec une autre. Par exemple, si vous voulez savoir pourquoi le fer rouille, vous pouvez le demander à un chimiste, il pourra vous répondre car il s’agit de l’étude de l’évolution du fer dans un milieu donné (l’eau par exemple). En fait, il vous expliquera que l’oxydation du fer, puisque c’est de cela dont il s’agit, est une forme de combustion lente mettant en jeu des échanges d’électrons entre le métal et l’oxygène contenu dans l’eau.
On peut également considérer la chimie comme de la cuisine. On associe plusieurs choses (les “ingrédients” s’appellent les réactifs), et on observe le résultat final (les “plats cuisinés” s’appellent les produits). On parle même de “laboratoire”, de “paillasse” qui sont des termes communs aux deux disciplines.
J’avoue que c’est une image un peu grossière, mais je l’aime bien… Et pourtant je fus un bon chimiste mais suis un piètre cuisinier.
À l’époque actuelle, la chimie est utile dans tellement de domaines que je ne pourrai pas tous vous les citer. Sachez que maintenant, la chimie est bien présente dans notre vie quotidienne.
Le plastique en est un bon exemple : il est partout celui-là. Regardez votre télécommande, votre chaîne hi-fi, votre téléphone, ou peut-être même la chaise sur laquelle vous êtes assis. C’est bourré de plastique ! Et d’où vient cette matière magique ? Des laboratoires bien sûr !
Mais ce n’est pas tout ! La chimie est présente dans bien d’autres domaines. Par exemple :
Médecine et santé : fabrication de médicaments, …
Énergie et électricité : piles électriques, centrales nucléaires, …
Cosmétique : parfum, rouge à lèvres, maquillage, …
Agriculture : engrais, pesticides, …
Agroalimentaire : arômes de synthèse, …
Divers : colle, peinture, savon, …
Et même dans votre corps : rien qu’en respirant, vous faites de la chimie !
Bref, la chimie est loin d’être inutile et est présente partout dans notre monde.
Nous allons découvrir dans les futurs articles quelques applications amusantes de la chimie.
Affaire à suivre !